Quelle: http://derstandard.at/1362108241498/Krebskiller-aus-der-Muttermilch
Die Krebstherapie macht beträchtliche Fortschritte - und trotzdem ist nach wie vor die Hälfte aller Krebserkrankungen nicht vollständig heilbar. Die Erkrankung kann noch Jahre nach der Behandlung erneut auftreten, es können sich Metastasen bilden, und nicht selten haben herkömmliche Therapien wegen ihrer mangelhaften Treffsicherheit massive Nebenwirkungen.
Ein großes Ziel der Krebsforschung ist deshalb die Entwicklung spezifischer Therapien, die nur die Krebszellen vernichten, die gesunden Zellen aber nicht in Mitleidenschaft ziehen. Wissenschafter der Abteilung für Biophysik am Institut für Molekulare Biowissenschaften an der Karl-Franzens-Universität Graz verfolgen eine neue Strategie, in der sie menschliche Immunabwehrpeptide für eine zielgenaue Bekämpfung von Krebszellen fit machen.
Ladungsunterschiede
Eines dieser kleinen Proteine, das die Grazer Forscher in Vorstudien bereits sehr genau unter die Lupe genommen haben, ist das in der Muttermilch vorkommende Lactoferricin. Dieses natürliche Immunabwehrpeptid mit seiner antibakteriellen und antiseptischen Wirkung zerstört Krebszellen, ohne das gesunde Gewebe anzugreifen. Die Peptide lösen die den Krebszellen eigene Zelltodhemmung auf und leisten damit praktisch Beihilfe zum Krebszellsuizid. Die Ursache ihrer Treffsicherheit liegt, wie die Forscher in einem vom Wissenschaftsfonds FWF geförderten Projekt belegen konnten, in Ladungsunterschieden von Peptiden und der Membranoberfläche von Krebszellen. Die positiv geladenen Peptide zielen aufgrund der elektrostatischen Wechselwirkung auf die negativ geladene Membranoberfläche der Krebszelle und dringen in sie ein, während sie gesunde Zellen mit ihren neutralen Lipiden in der äußeren Zellmembranschicht ignorieren.
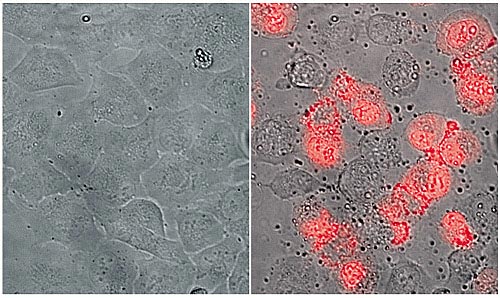
"Ich und meine Mitarbeiterin Sabrina Riedl konnten nachweisen, dass Krebszellen das negativ geladene Phospholipid Phosphatidylserin (PS) im Gegensatz zu gesunden Zellen an der Außenseite ihrer Membran tragen", erklärt die Projektleiterin Dagmar Zweytick. Bei verschiedenen Prozessen, etwa bei der Bildung einer Krebszelle, klappt nämlich das negativ geladene Lipid nach außen und gibt auf diese Weise einen zuverlässigen Biomarker ab. Dieser in der Fachwelt bis zur Veröffentlichung der Grazer Erkenntnisse oft angezweifelte Umstand ist von enormer Tragweite, da er den oft schwierigen Weg für eine zielgenaue Krebsbehandlung aufzeigt.
"Tatsächlich fanden wir dieses negativ geladene Lipid nicht nur auf der Zellmembran von Zelllinien verschiedener Krebsarten, sondern auch bei Metastasenzellen und primären Krebszellen", betont Zweytick. Zudem deutet die Studie an unterschiedlichen Hauttumoren darauf hin, dass der exponierte PS-Gehalt mit der Bösartigkeit des Gewebes zunimmt.
Gehirntumor und Melanom
"In unseren biophysikalischen Untersuchungen konnten wir auch beweisen, dass die wirksamen und für Krebszellen selektiven Peptide tatsächlich PS als Angriffspunkte nutzen." Auf der Basis dieser umwälzenden Erkenntnisse haben die Forscher das Krebsabwehrpeptid Lactoferricin für seinen Kampf gegen zwei besonders schwer therapierbare Krebsarten aufgerüstet: den bösartigen Gehirntumor (Glioblastom) und das maligne Melanom, den metastasierenden Hautkrebs.
"Wir haben die Peptide zunächst in Modellstudien, dann in Zellkulturen für diese bislang unheilbaren Krebserkrankungen optimiert", berichtet Zweytick. "Dafür haben wir zwei vom menschlichen Lactoferricin abgeleitete Peptid-Wirkstoffe ausgewählt und so verändert, dass sie eine spezifische Toxizität gegenüber Glioblastom und Melanom entwickelten." Mittlerweile ist die Arbeit so weit fortgeschritten, dass die humanen Peptidderivate im aktuellen, ebenfalls vom FWF finanzierten Projekt gemeinsam mit Beate Rinner von der Medizin-Uni Graz an Mäusen erprobt und weiter verbessert werden können.
Für den Kampf gestärkt
Warum aber müssen die natürlichen Peptide überhaupt verändert werden? " Da die Peptide in der Natur nur zur Abwehr der ersten Gefahr durch Bakterien, Viren oder eben Krebs ausgestattet sind, würden sie den Kampf etwa gegen einen massiven Tumor verlieren", erläutert die Wissenschafterin. "Durch unsere Optimierungen wollen wir die Wirkung der Peptide entsprechend verstärken und gleichzeitig verhindern, dass der Einsatz höherer Dosen auch für gesunde Zellen toxisch wird."
Verglichen mit Chemotherapien, haben humane Peptidderivate zur Behandlung von Krebs enorme Vorteile: "Chemotherapien", sagt Zweytick, " wirken meist auf schnell wachsende Zellen - und das sind bedauerlicherweise nicht nur die Krebszellen. Deshalb kommt es auch oft zu starken Nebenwirkungen. Das kann man mit Peptiden vermeiden, da sie nur Zellen angreifen, die das negativ geladene PS außen tragen." Selbst Krebsarten, die wie das maligne Melanom gegen Chemotherapie weitgehend resistent sind, sollen mithilfe optimierter Peptide therapierbar werden. Und noch einen großen Vorteil haben die Antitumorpeptide: Sie können sogar mutierte Krebszellen mit geänderter Erbinformation finden.
Der Weg dieser bahnbrechenden Erkenntnisse in die Kliniken ist allerdings noch ein relativ weiter: "Ein erster Schritt ist durch die Einreichung einer europäischen Patentanmeldung zwar getan, wir müssen jedoch noch die Wirksamkeit und Stabilität der Peptide verbessern, sodass sie wirklich alle Krebszellen erfassen können", dämpft Dagmar Zweytick allzu ungeduldige Erwartungen. Sind diese Herausforderungen bewältigt, soll das wertvolle Wissen an eine Pharmafirma übergeben werden - zur Durchführung der sehr teuren klinischen Studien. (Doris Griesser, DER STANDARD, 13.03.2013)